近日,清华大学免疫学研究所、清华大学医学院基础医学系祁海课题组在《Cell Insight》期刊在线发表了题为“A role for Hes1 in constraining germinal center B cell formation”的研究论文。文章首次揭示了Notch信号通路下游靶基因Hes1对生发中心反应的负向调控作用。
生发中心是二级淋巴器官中形成的供B细胞进行亲和力成熟的微型结构,是高亲和力记忆B细胞与长寿浆细胞产生的主要场所。生发中心反应在对抗感染与针对疫苗免疫形成免疫记忆的过程中有重要作用,但当其控制不当时也可能造成自免疫疾病与肿瘤的发生。因此,对于生发中心调控机制的深入研究有着重要意义。
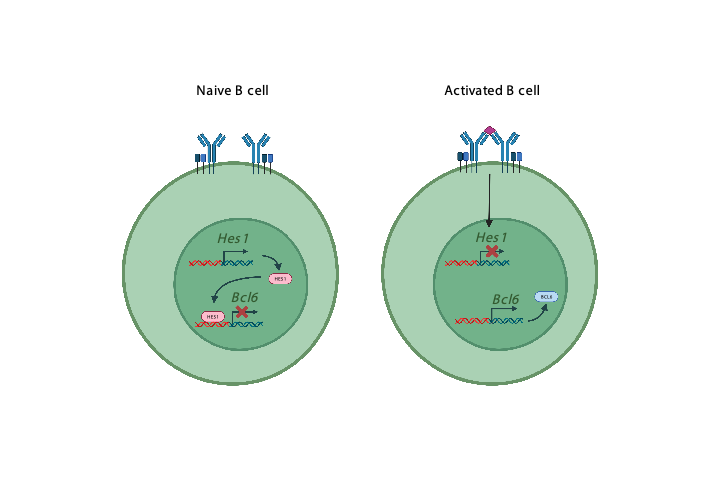
图1. Hes1负向调控生发中心反应机制示意图。
生发中心的产生依赖于B细胞中转录因子Bcl6的上调,但调控这个过程的机制并不完全明确。在本课题中,研究者们发现Hes1可通过负向调控Bcl6的表达对B细胞参与生发中心反应进行约束(图1)。在B细胞中缺失Hes1的小鼠脾脏中,自发与免疫后形成的生发中心较野生型小鼠均有显著上升(图2)。Hes1表达本身受到B细胞受体信号的负调控,但其缺陷并不影响生发中心B细胞的激活、增殖与凋亡,提示其可能在生发中心起始阶段发挥作用。与此相吻合的是,在免疫后初期从B细胞中诱导性的敲除Hes1可增强生发中心反应,并相应的提升生发中心来源的浆细胞的丰度,但在生发中心反应充分建立后再进行敲除则没有这样的效果。
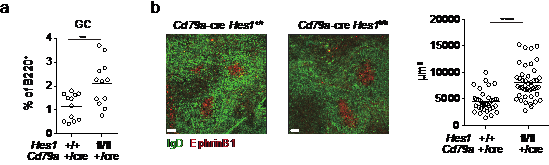
图2. 免疫后第7天,流式结果(a)与免疫荧光结果(b)均显示从B细胞中条件性敲除Hes1后小鼠脾脏生发中心显著增大
通过对生发中心前体B细胞进行分析,作者们发现在同一小鼠中Hes1缺陷的B细胞在免疫早期增殖更多,并能更快的上调Bcl6表达。由于Bcl6启动子上具有潜在可被Hes1结合的位点,作者们猜想后者对前者可能有直接调控作用。在进一步研究中,作者们利用荧光报告实验证明HES1对于Bcl6启动子确实具有抑制作用,而这样的作用依赖于HES1的bHLH DNA结合域(图3)。此外,在体外激活的B细胞中过表达Hes1可下调Bcl6的表达。

图3. 荧光报告实验显示HES1对于Bcl6启动子的抑制作用依赖于其bHLH结构域
总体而言,这些结果描述了Hes1调控Bcl6表达的新机制,揭示Notch通路与B细胞受体信号通路的协作模式,并深化了人们对于生发中心反应起始调控的认识,为理解体液免疫记忆的形成与自免疫疾病的发生提供了新视角。
祁海教授为本文的通讯作者;清华大学医学院已毕业的邵星星博士是文章的第一作者;清华大学医学院助理研究员刘欣也为论文作出了贡献。该课题得到了国家自然科学基金与清华-北大生命联合中心的支持。

版权所有©2017 清华大学免疫学研究所
地址:清华大学医学楼D302,北京,100084
电话:010-62776420 传真:010-62776420
