免疫系统既要行使免疫防御功能,但又要保持自身耐受,即不攻击自身。具有吞噬功能的巨噬细胞为何不“吃掉”自体健康细胞是重要免疫学问题。目前认为决定巨噬细胞能否发挥吞噬功能主要依赖其表面的活化型“食我”受体和抑制型“别食我”受体。目前公认的巨噬细胞表面“别食我”受体是SIRPa,它识别广泛表达的CD47,触发含有SH2结构域的磷酸酶(SHP)-1和/或SHP-2的信号,从而抑制巨噬细胞介导的吞噬作用。因此SIRPa/CD47被认为是一种免疫稽查点分子,多种靶向SIRPa/CD47抗体药物已经进入临床试验。尽管如此,SIRPa或CD47缺陷小鼠并没有或只有轻微的巨噬细胞介导的自身免疫现象,提示机体可能存在其它重要的“别食我”受体未被发现。
2022年1月21日,清华大学免疫学研究所/医学院董忠军课题组在《科学-免疫学》(Science Immunology)发表题为“SLAMF3 and SLAMF4 are immune checkpoints that constrain macrophage phagocytosis of hematopoietic tumors” 研究论文。首次报道淋巴细胞活化信号分子(SLAM)家族是一种新型“别食我”受体,负责抑制巨噬细胞吞噬自身健康血液细胞,当该家族受体缺失时,会引起严重的血液细胞移植排斥。
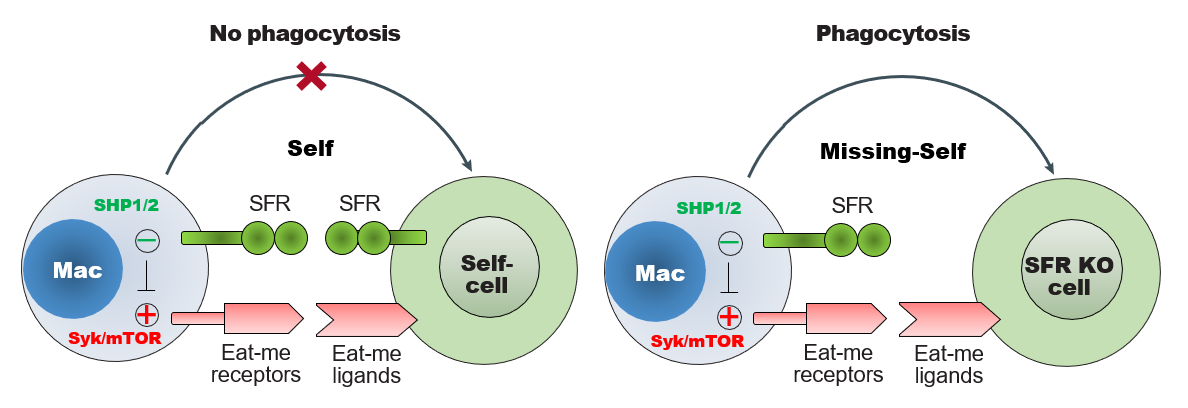 图1 SLAM家族受体抑制巨噬细胞吞噬的新机制研究
图1 SLAM家族受体抑制巨噬细胞吞噬的新机制研究
SLAM家族受体由7种同源识别的免疫受体组成,它们通常招募下游SAP家族蛋白传递活化信号,调节多种免疫反应,如NK细胞活化,NK-T细胞发育和抗体产生等。人类SAP基因突变会导致严重的免疫缺陷性疾病XLP1。本研究首次揭示了SLAM家族受体可以通过SHP1/SHP2传递SAP家族非依赖的抑制信号,削弱巨噬细胞表面“食我”受体信号,如Syk和mTOR,从而阻止巨噬细胞吞噬自身健康血液细胞(图1)。SLAM家族受体只表达于血液系统细胞表面,常被用作区分造血干细胞和其它造血前体细胞的标志物,该研究首次证明该家族受体类似于CD47,可能是一种新的“自我”分子,特异地抑制巨噬细胞对自身血液的吞噬,维持巨噬细胞耐受。因此,SLAM家族受体可能代表一种血液组织特异性的“别食我”受体。
该研究具有重要的临床意义,嗜血细胞综合征是一种致死率较高的疾病,临床上通常出现全血细胞减少,其发病机制与吞噬细胞异常地吞噬正常机体细胞有关。本研究发现人嗜血细胞综合征患者血液SLAM家族受体表达显著降低,提示SLAM家族受体表达量下调可能是噬血细胞综合征的发病新机制。
该研究具有潜在的转化价值,肿瘤细胞高表达“别食我” 配体可导致肿瘤免疫逃避,譬如肿瘤细胞上调CD47表达可以抑制巨噬细胞的吞噬功能。很多造血系统肿瘤通常也高表达SLAM家族受体,该研究发现阻断SLAM家族受体可以增加巨噬细胞清除血液系统肿瘤,因此,SLAM家族受体有望成为新的免疫稽查点分子,该研究为肿瘤免疫治疗提供新的靶点。
清华大学医学院李丹博士为该论文第一作者,清华大学免疫所/医学院董忠军博士和复旦大学医学院陈莎莎博士为通讯作者。该工作得到北京地坛医院曾辉博士、上海交通大学医学院王静博士、吉林大学附属第一医院杨永广博士、华中科技大学基础医学院武宁博士和暨南大学杨美香博士的大力支持。清华大学实验动物中心为该课题系列动物模型制备提供了不可或缺的帮助。该研究得到了国家自然科学基金委重点课题、清华大学-北京大学生命联合中心和清华大学免疫所的经费支持。
董忠军课题组致力于天然免疫细胞活化和耐受机制研究,特别在NK细胞活化和耐受领域取得了多项进展。该发现揭示了SLAM家族受体的全新功能,为课题组开辟新的研究方向,欢迎有志于该方向的青年才俊加入团队。
原文链接:
https://www.science.org/doi/10.1126/sciimmunol.abj5501

版权所有©2017 清华大学免疫学研究所
地址:清华大学医学楼D302,北京,100084
电话:010-62776420 传真:010-62776420
