
膀胱癌(Bladder Cancer)是全球第十大常见癌症,年新发病例基数庞大。近半患者治疗后出现复发或转移,晚期患者五年生存率不足10%,其核心治疗瓶颈在于肿瘤微环境(TME)的免疫抑制机制尚未明确。近日,清华大学医学院免疫学研究所吴励团队、国家蛋白质科学中心(北京)朱云平团队与中国医学科学院肿瘤医院邢念增团队合作,在Lancet子刊《eBioMedicine》发表题为“High-resolution transcriptome atlas of bladder cancer highlights the functional myeloid subsets in modulating immune microenvironment”的研究论文,首次揭示TREM2high巨噬细胞与CMA1high肥大细胞在膀胱癌中的代谢重编程机制,并提出靶向TREM2/APP可重塑膀胱癌免疫微环境。
该研究对11例膀胱癌患者的配对癌和癌旁组织进行了单细胞转录组测序分析(图1a),通过对免疫细胞亚群的精细聚类与功能注释,为膀胱癌免疫调控提供全新见解,并通过小鼠膀胱癌模型对发现的靶点进行了验证。该研究的重要发现包括:
1. TREM2high巨噬细胞与CMA1high肥大细胞在膀胱癌组织中发生显著代谢重编程,小鼠模型中敲除Trem2基因可重塑免疫微环境;
2. CMA1high肥大细胞富集提示膀胱癌不良预后,而CD1C+树突状细胞的存在可作为保护性的预后标志物;
3. 通过构建四种免疫细胞模块集群(Immune Cellular Modules),为膀胱癌精准免疫分型提供新的工具(图1b);
4. 细胞互作网络分析发现APP信号轴(Amyloid Precursor Protein,与阿尔茨海默症相关蛋白同源)的关键作用;并建立了一种原位小鼠膀胱癌模型,验证了敲低APP基因显著抑制肿瘤进展(图1c)。
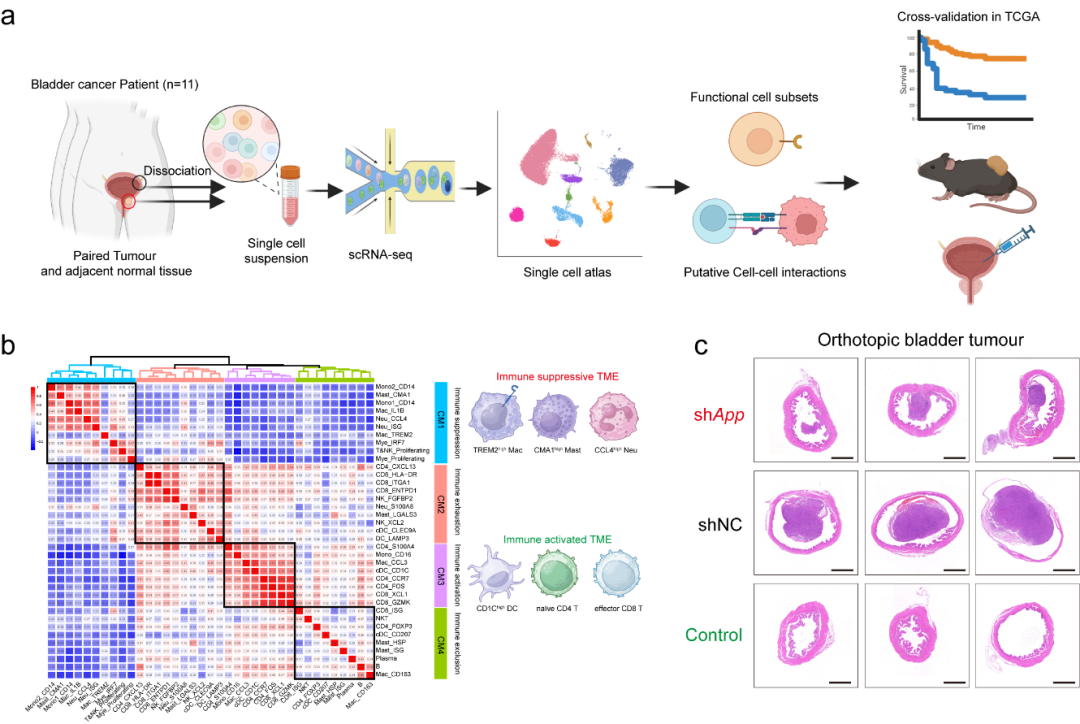
图1. 膀胱癌单细胞全景的建立、免疫细胞模块集群的建立和小鼠原位膀胱癌模型研究
清华大学医学院免疫学研究所博士生刘家琛,史真(已毕业),中国医学科学院肿瘤医院李亚健主治医师,国家蛋白质科学中心马洁副研究员和北京安诺优达姚佳英为本文共同第一作者。清华大学医学院吴励教授和张建宏助理研究员,国家蛋白质科学中心(北京)朱云平教授和中国医学科学院肿瘤医院邢念增副院长为本文共同通讯作者。相关工作获得了国家自然科学基金、科技部重点研发计划和清华北大生命科学联合中心的基金支持。

上图为研究团队受邀设计的封面图,展现了膀胱癌免疫微环境的研究及发现:
1. 整体轮廓——展现膀胱器官的形态,象征研究聚焦于膀胱组织微环境;
2. 探索过程——潜水艇代表对免疫微环境的系统性探索;
3. 图中两侧地貌差异呈现了膀胱癌导致的组织结构畸变:左侧翠绿生态区(平整珊瑚/繁茂水草/气泡)象征癌旁正常组织及抑癌因子(如CD1C+ DC、T细胞);右侧暗红病变区(崎岖礁石/散落的小花/凶恶的小鱼)代表癌组织及促癌因子(如TREM2、APP);
文章全文在线链接:
https://doi.org/10.1016/j.ebiom.2025.105801
吴励课题组

清华大学免疫所吴励教授课题组长期致力于髓系免疫细胞,尤其是树突状细胞(DC)和巨噬细胞在发育、疾病等过程中的基础研究和应用,探索髓系免疫细胞的分化、激活和迁移等过程的关键调控机制。现因课题发展需要,招聘博士后研究员(2名)。我们热切期待对免疫学研究充满热情、有志于在顶尖平台上追求卓越的您加入我们研究团队!

Copyright © 2017 Institute for Immunology Tsinghua University
Contact Address: Room D302, Medical Science Building, Tsinghua University, Beijing 100084, China
Tel: (86) 10-62776420 Fax: (86) 10-62776420
