脑膜作为包裹中枢神经系统的保护性屏障,近年来被证实是一个活跃的免疫调控枢纽。尽管肥大细胞作为组织驻留的免疫哨兵已知存在于脑膜,其在病毒感染过程中的具体功能仍不清楚。
为探究这一问题,研究团队首先绘制了脑膜肥大细胞的时空分布图谱,发现其在小鼠断奶后经历关键成熟阶段,并定位于脑膜巨噬细胞、血管及神经纤维周围,提示其可能参与特定的生理与免疫调节过程。此外,团队基于Tpsb2基因构建了新型工具小鼠品系Tpsb2-CreERT2,实现了对肥大细胞的高效、特异性及非毒性标记,为相关细胞功能研究提供了重要手段。
在功能层面,研究人员利用淋巴细胞性脉络丛脑膜炎病毒(LCMV)感染模型,结合单细胞RNA测序和全脑膜免疫荧光染色分析,发现脑膜肥大细胞在病毒感染后被显著激活,表现为转录组水平上调和脱颗粒反应增强。进一步通过细胞缺失、药理遗传学及光遗传学等多种策略对肥大细胞进行功能干预,研究团队从多角度验证了其在抗病毒免疫中不可或缺的作用。
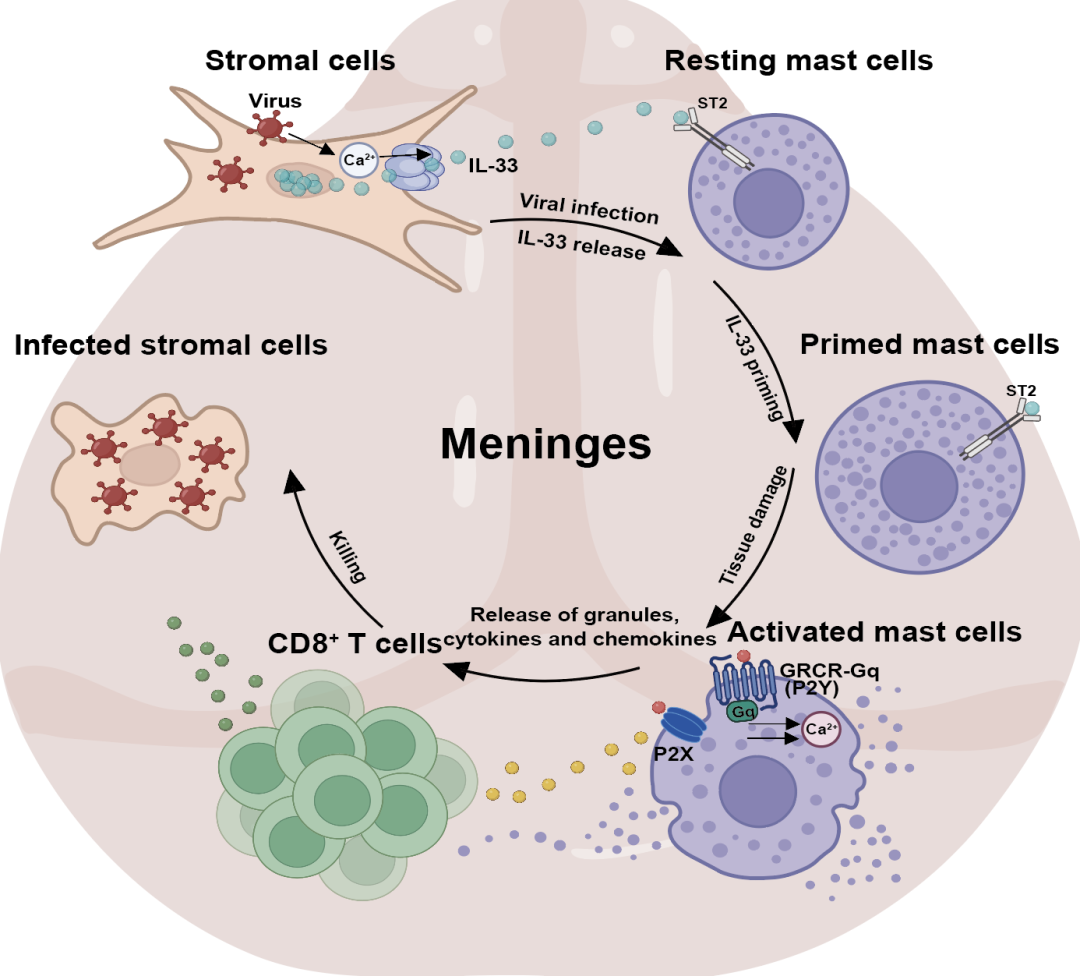
在机制层面,研究揭示基质细胞在病毒感染早期释放IL-33,肥大细胞则通过其表面受体ST2接收该信号,从而增强自身活化并促进脑膜抗病毒免疫。更有趣的是,在感染后期,基质细胞进一步释放ATP,经由P2X7受体激活肥大细胞。IL-33与ATP双信号协同作用,显著增强了肥大细胞中多种细胞因子与趋化因子的表达,并促进其脱颗粒,进而有效招募并激活CD8⁺ T细胞,最终强化脑膜的抗病毒免疫应答。
综上所述,该研究不仅重新定位了肥大细胞在脑膜抗病毒免疫中的重要地位,还深入阐释了其与基质细胞之间的精确互作机制。这一发现拓展了人们对中枢神经系统屏障免疫的认识,也为针对病毒感染及相关神经炎症性疾病的治疗策略开发提供了新思路。
清华大学基础医学院、免疫学研究所曾文文教授与遵义医科大学附属医院曹芳教授为本文的共同通讯作者。清华大学基础医学院博士生李庆庆、陈维佳和孙梦雪为共同第一作者。清华大学博士生倪鑫波与遵义医科大学附属医院冉启山教授亦对本研究作出重要贡献。研究过程中得到胡小玉教授的宝贵建议,并感谢董忠军教授、陈晔光教授、刘万里教授及胡小玉教授惠赠小鼠品系。
本研究受国家重点研发计划、国家自然科学基金、清华-北大生命科学联合研究中心、清华大学免疫学研究所、清华大学基础医学院以及山西医科大学—清华大学医学院前沿医学协同创新中心等项目和机构支持。
原文链接:
IITU丨清华免疫

Copyright © 2017 Institute for Immunology Tsinghua University
Contact Address: Room D302, Medical Science Building, Tsinghua University, Beijing 100084, China
Tel: (86) 10-62776420 Fax: (86) 10-62776420
