- 清华大学免疫所郭晓欢课题组揭示3型天然淋巴样细胞调控肠道菌群新机制
清华大学基础医学院免疫所郭晓欢课题组在Nature Microbiology杂志上在线发表题为ILC3s regulate the gut microbiota via host intestinal galactosylation to limit pathogen infection in mice的研究论文,揭示了3型天然淋巴样细胞(group 3 innate lymphoid cells, ILC3s)通过调控肠道上皮细胞糖基化及菌群代谢物抵御病原体感染的关键机制。该研究利用小鼠肠道感染模型,首次阐明了ILC3s介导的糖基化调控、肠道菌群与致病菌之间的复杂互作网络,为肠道免疫调控及抗感染治疗提供了全新视角。
宿主免疫细胞与肠道共生菌群的协同作用是维持肠道稳态、抵御病原体入侵的重要防线,但其分子与细胞机制尚未得到充分阐明。研究团队利用啮齿类柠檬酸杆菌(Citrobacter rodentium)小鼠感染模型,发现ILC3s可以通过影响肠道共生菌嗜黏蛋白阿克曼菌(Akkermansia muciniphila)及其代谢物琥珀酸(succinate)显著增强宿主对肠道感染的抵抗力。
机制研究表明,ILC3s通过分泌细胞因子IL-22, 调控小鼠肠道上皮细胞半乳糖基化水平,从而维持菌群稳态。当ILC3s缺失时,肠道上皮细胞半乳糖基化水平异常增高,导致肠道黏液层中A. muciniphila过度扩增。进一步研究发现,该菌及其代谢产物琥珀酸可以经四碳二羧酸转运蛋白(DcuB)显著上调致病菌毒力因子tir和ler的表达,增强病原菌定植能力,最终加剧宿主感染。
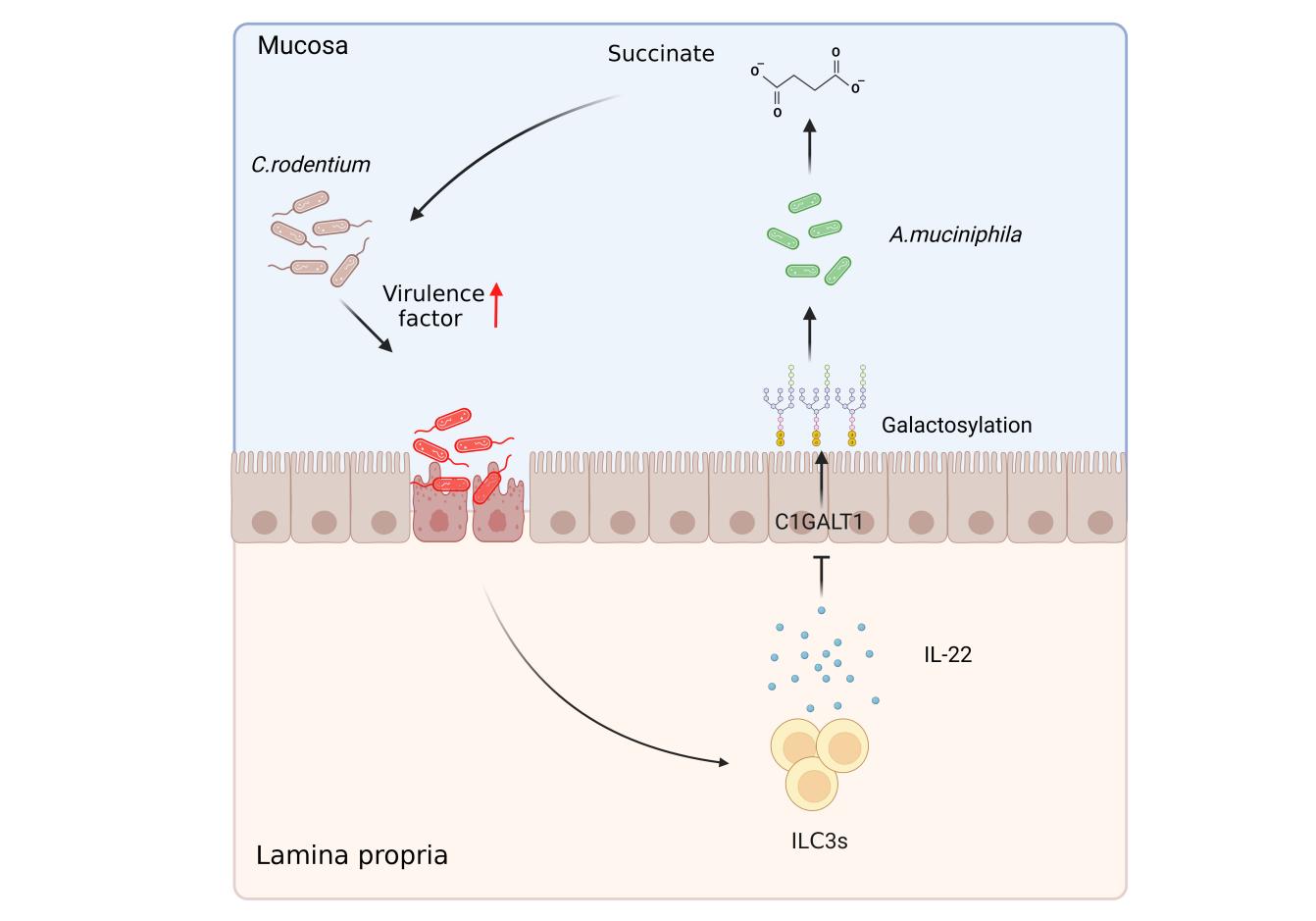
本研究建立了“ILC3s-肠道糖基化-菌群代谢-病原体毒力”的级联调控轴,这一发现不仅阐释了宿主免疫系统如何通过精细调控菌群及其代谢维持肠道黏膜稳态抑制感染的新机制,也为靶向菌群及其代谢干预相关疾病坚定了理论基础。同时,A. muciniphila是近年来颇受产业界关注的明星益生菌,本研究揭示其在过度增殖的情况下具有破坏肠道稳态的风险,提示了益生菌使用的安全性问题。
清华大学基础医学院助理研究员王文彦和博士生李娜为论文共同第一作者。清华大学基础医学院副教授、免疫学研究所研究员郭晓欢和助理研究员王文彦为本文的共同通讯作者。本研究得到了清华大学医学院傅阳心教授、胡小玉教授、裘莹教授和张敬仁教授的重要支持。清华大学基础医学院已毕业博士生许红凯、李奕平、欧加尧、张敬和博士后魏思婷、郝嘉成以及集萃药康的董力友博士为本项研究做出了重要贡献。本研究得到了国家自然科学基金项目、国家重点研发计划项目、北京市自然科学基金项目、山西医科大学-清华大学医学院前沿医学协同创新中心以及清华大学免疫学研究所等的支持。
原文链接:https://www.nature.com/articles/s41564-025-01933-9

Copyright © 2017 Institute for Immunology Tsinghua University
Contact Address: Room D302, Medical Science Building, Tsinghua University, Beijing 100084, China
Tel: (86) 10-62776420 Fax: (86) 10-62776420
- WeChat sweep add attention


